萃取:
利用物质在两种互不相溶(或微溶)的溶剂中溶解度或分配系数的不同,使物质从一种溶剂内转移到另外一种溶剂中。经过反复多次萃取,将绝大部分的化合物提取出来。
常见萃取剂:甲苯,二氯甲烷,三氯甲烷,汽油,乙醚,直馏汽油,正丁醇,四氯化碳。要求:萃取剂和原溶剂互不混溶。萃取剂和溶质互不发生反应。溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度。
萃取与其他分离溶液组分的方法相比,优点在于常温操作,节省能源,不涉及固体、气体,操作方便。萃取在如下几种情况下应用,通常是有利的:①料液各组分的沸点相近,甚至形成共沸物,为精馏所不易奏效的场合,如石油馏分中烷烃与芳烃的分离,煤焦油的脱酚;②低浓度高沸组分的分离,用精馏能耗很大,如稀醋酸的脱水;③多种离子的分离,如矿物浸取液的分离和净制,若加入化学品作分部沉淀,不但分离质量差,又有过滤操作,损耗也大;④不稳定物质。
化学学习——萃取与分液
1,萃取原理: 利用混合物中一种溶质在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来。
2,萃取进行的条件: 萃取剂和溶液中的溶剂要互不相溶、且密度有一定的差别,溶质在萃取剂中的溶解度要比在原溶剂中的溶解度大。
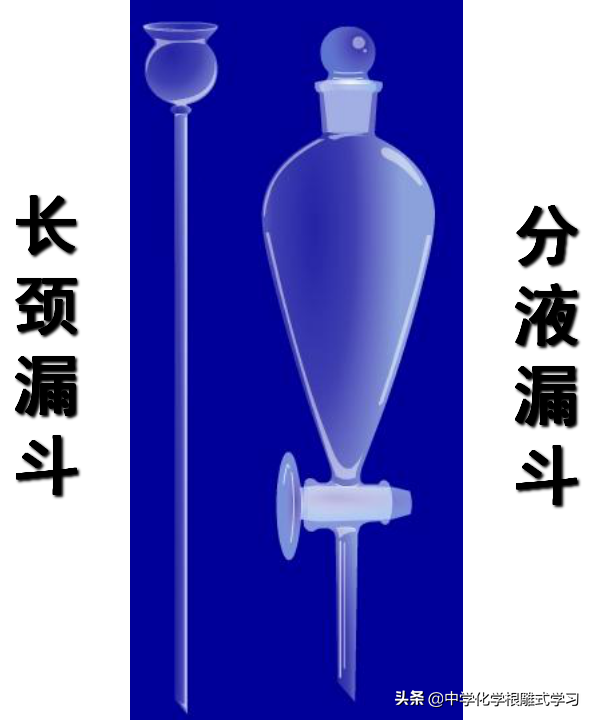
3,萃取常用的仪器:分液漏斗(不需要长颈漏斗)。
4,实验步骤:装液——振荡——静置——分液。
5,注意事项:
(1)振荡时,要不断放气,以减小漏斗内的压强。
(2)先将下层液体从下口流出,再将上层液体从上口倒出。
(3)分液时须将分液漏斗上的玻璃塞打开,或使玻璃塞上的凹槽(或小孔)对准漏斗上的小孔。
(4)漏斗颈的下端要紧贴烧杯的内壁。
(5)振荡时,须不断放气,以减少分液漏斗内的气压。
(6)萃取原则:少量多次。
(7)选择合适的萃取剂。
6,萃取、分液操作
萃取原液互不溶,质溶程度不相同。
充分振荡再静置,下放上倒记分明。